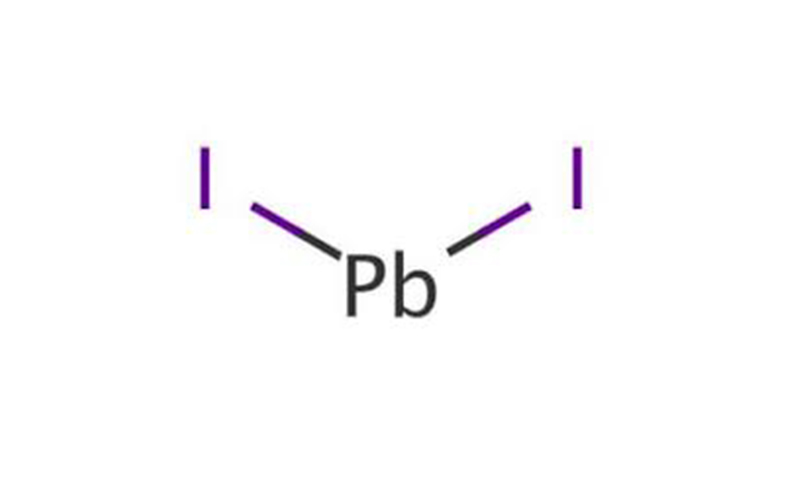
Lead(II) iodida10101-63-0
Sifat Kimia Timbal (II) iodida
| Titik leleh | 402 °C (menyala) |
| Titik didih | 954 °C (menyala) |
| Kepadatan | 6,16 g/mL pada suhu 25 °C (menyala) |
| Fp | 954 °C |
| suhu penyimpanan. | Simpan di tempat gelap, Atmosfer lembam, Suhu kamar |
| Kelarutan | Larut dalam larutan pekat alkali iodida dan natrium tiosulfat. Tidak larut dalam alkohol dan asam klorida dingin. |
| bentuk | Beads |
| warna | Kuning hingga oranye |
| Berat Jenis | 6.16 |
| Kelarutan Air | Larut sebagian dalam air. Larut bebas dalam larutan natrium tiosulfat. Larut dalam larutan alkali iodida terkonsentrasi. Tidak larut dalam alkohol dan HCl dingin.Larut dalam larutan pekat alkali iodida dan natrium tiosulfat. Tidak larut dalam alkohol dan asam klorida dingin. |
| Sensitivitas hidrolitik | 0: membentuk larutan berair yang stabil |
| λmaks | 539nm (rapi) (menyala) |
| Peka | Sensitif Cahaya |
| Kepadatan | 6.16 |
| Konstanta Produk Kelarutan (Ksp) | pKsp: 8.01 |
| Batas paparan | ACGIH: TWA 0,05 mg/m3; TWA 0,01 ppm NIOSH: IDLH 100 mg/m3; TWA 0,050 mg/m3 |
| Stabilitas: | Kandang. Dapat berubah warna saat terkena cahaya. |
| InChIKey | RQQRAHKHDFPBMC-UHFFFAOYSA-L |
Informasi Keselamatan
| RIDADR | PBB 2291 6.1/PG 3 |
| WGK Jerman | 3 |
| TSCA | Ya |
| Kelas Bahaya | 6.1 |
| Grup Pengepakan | III |
| Kode HS | 28276000 |
Penggunaan Dan Sintesis Iodida Timbal (II)
| Deskripsi | Timbal (II) iodida (rumus kimia: PbI) adalah sejenis garam anorganik. Itu muncul sebagai padatan kristal kuning cerah. Ini memiliki beberapa aplikasi khusus seperti pembuatan sel surya, sinar-X, dan detektor sinar gamma. Selain itu, juga dapat digunakan sebagai pigmen cat untuk digunakan dalam seni untuk perunggu dan ubin mosaik seperti emas. Ini biasanya dapat disintesis melalui reaksi perpindahan ganda antara kalium iodida KI dan timbal (II) nitrat Pb(NO3)2 dalam larutan air. Timbal (II) asetat dan natrium iodida juga dapat digunakan sebagai pengganti timbal nitrat dan kalium iodida, masing-masing. Atau, dapat diproduksi melalui reaksi antara uap yodium dan timbal cair. Ini juga digunakan dalam pencetakan dan fotografi. Namun, itu berbahaya bagi lingkungan, dan harus diperhatikan untuk membatasi penyebaran ke lingkungan. |
| Referensi | https://en.wikipedia.org/wiki/Lead(II)_iodide https://pubchem.ncbi.nlm.nih.gov/compound/Lead_II__iodide#section=Top |
| Deskripsi | Lead Iodida adalah bubuk berat, kuning cerah, tidak berbau. Identifikasi Bahaya (berdasarkan Sistem MRating NFPA-704): Kesehatan 2, Mudah Terbakar 0, Reaktivitas 0. Larut dalam air. |
| Sifat kimia | Iodida timbal adalah bubuk berat, kuning cerah, tidak berbau. |
| Sifat fisik | Kristal heksagonal kuning; kepadatan 6,16 g / cm3; meleleh pada suhu 402 °C; menguap pada 954°C; terurai pada suhu 180°C saat terkena cahaya hijau; sedikit larut dalam air (0,44 g/L pada 0°C dan 0,63 g/L pada 20°C); Ksp 8,49×10-9 pada 25°C; larut sebagian dalam air mendidih (4,1 g/L pada 100 °C); tidak larut dalam etanol; larut dalam larutan alkali dan alkali logam iodida. |
| Menggunakan | Iodida timbal (II) digunakan sebagai bahan detektor untuk foton berenergi tinggi termasuk sinar-x dan sinar gamma. Ini digunakan dalam fotografi, percetakan, emas mosaik, dan perunggu. Ini menunjukkan sifat feroelastik dan memiliki efisiensi dalam menghentikan sinar-X dan sinar gamma, yang memberikan stabilitas lingkungan yang sangat baik. |
| Menggunakan | Digunakan dalam perunggu, percetakan, fotografi, pensil emas, dan emas mosaik. |
| Persiapan | Timbal diiodida dibuat dengan mencampurkan larutan berair timbal nitrat atau timbal asetat dengan larutan kalium atau natrium iodida atau asam hidriodik, diikuti dengan kristalisasi. Produk dimurnikan dengan rekristalisasi. Pb2+(aq) + 2Iˉ (aq) → PbI2(s). |
| Deskripsi Umum | Timbal iodida muncul sebagai padatan kristal kuning. Tidak larut dalam air dan lebih padat dari air. Bahaya utama adalah ancaman terhadap lingkungan. Langkah-langkah segera harus diambil untuk membatasi penyebaran ke lingkungan. Digunakan dalam pencetakan dan fotografi, untuk menyemai awan dan kegunaan lainnya. |
| Reaksi Udara & Air | Sedikit larut dalam air. |
| Profil Reaktivitas | Iodida timbal(II) memiliki daya oksidasi atau pereduksi yang lemah. Namun reaksi redoks masih bisa terjadi. Sebagian besar senyawa dalam kelas ini sedikit larut atau tidak larut dalam air. Jika larut dalam air, maka larutannya biasanya tidak sangat asam atau sangat basa. Senyawa ini tidak reaktif air. Sensitif terhadap cahaya |
| Bahaya | Timbal diiodida beracun jika tertelan. Gejalanya adalah keracunan timbal. |
| Bahaya kesehatan | Gejala awal keracunan timbal melalui inhalasi atau konsumsi paling sering adalah gangguan pencernaan, kolik, sembelit, dll.; kelemahan, yang dapat berlanjut ke kelumpuhan, terutama pada otot ekstensor pergelangan tangan dan lebih jarang pergelangan kaki, terlihat pada kasus yang paling serius. Menelan dalam jumlah besar menyebabkan iritasi lokal pada saluran pencernaan. Nyeri, kram kaki, kelemahan otot, paresthesia, depresi, koma, dan kematian dapat terjadi dalam 1 atau 2 hari. Kontak dengan mata menyebabkan iritasi. |
| Potensi Paparan | Iodida timbal digunakan dalam perunggu, pensil emas; emas mosaik; percetakan, dan fotografi |
| Pertolongan pertama | Jika bahan kimia ini masuk ke mata, segera lepaskan lensa kontak dan segera irigasi setidaknya selama 15 menit, sesekali angkat kelopak atas dan bawah. Segera cari pertolongan medis. Jika bahan kimia ini menyentuh kulit, lepaskan pakaian yang terkontaminasi dan segera cuci dengan sabun dan air. Segera cari pertolongan medis. Jika bahan kimia ini telah terhirup, angkat dari paparan, mulailah pernapasan penyelamatan (menggunakan tindakan pencegahan universal, termasuk masker resusitasi) jika pernapasan telah berhenti dan CPR jika tindakan jantung telah berhenti. Pindahkan segera ke fasilitas medis. Ketika bahan kimia ini telah tertelan, dapatkan pertolongan medis. Berikan air dalam jumlah besar dan menginduksi. Jangan membuat orang yang tidak sadarkan diri muntah. Penangkal dan prosedur khusus untuk timbal: Orang dengan keracunan timbal yang signifikan terkadang diobati dengan CaEDTA saat dirawat di rumah sakit. Obat “pengkelat” ini menyebabkan aliran timbal dari organ tubuh ke dalam darah dan ginjal, dan dengan demikian memiliki bahaya tersendiri, dan hanya harus diberikan oleh tenaga medis yang sangat berpengalaman dalam kondisi yang kurang terkontrol dan pengamatan yang cermat. Ca EDTA atau obat serupa tidak boleh digunakan untuk mencegah keracunan saat paparan berlanjut atau tanpa kontrol paparan yang ketat, karena kerusakan ginjal yang parah dapat terjadi. Catatan kepada dokter: Untuk keracunan parah BAL [British AntiLewisite, dithiopropanol (C3H8OS2)] telah digunakan untuk mengobati gejala toksik dari keracunan logam berat tertentu. Dalam kasus keracunan timbal, mungkin memiliki BEBERAPA nilai. Meskipun BAL dilaporkan memiliki margin keamanan yang besar, kehati-hatian harus dilakukan, karena efek toksik mungkin disebabkan oleh dosis yang berlebihan. Sebagian besar dapat dicegah denganprapengobatan dengan 1-efedrin sulfat (CAS: 134-72-5). |
| penyimpanan | Kode Warna—Biru: Bahaya Kesehatan/Racun: Simpan di lokasi racun yang aman. Sebelum bekerja dengan bahan kimia ini, Anda harus dilatih tentang penanganan dan penyimpanannya yang tepat. Timbal iodida harus disimpan untuk menghindari kontak dengan pengoksidasi (seperti perklorat, peroksida, permanganat, klorat, dan nitrat) dan logam aktif kimia (seperti kalium, natrium, magnesium, dan seng), karena terjadi reaksi kekerasan. Area yang diatur dan ditandai harus ditetapkan di mana bahan kimia ini ditangani, digunakan, atau disimpan tidak sesuai dengan Standar OSHA 1910.1045. Timbal iodida diatur oleh Standar OSHA, 1910.1025. Semua persyaratan standar harus diikuti. |
| Pengiriman | UN3288 Padatan beracun, anorganik, n.o.s., Kelas Bahaya: 6.1; Label: 6.1-Bahan beracun, Nama Teknis Diperlukan. UN3077 Zat berbahaya lingkungan, padat, n.o.s., Kelas bahaya: 9; Label: 9-Bahan berbahaya lain-lain, Nama Teknis Diperlukan |
| Metode Pemurnian | Ini mengkristal dari volume air yang besar. Kelarutan dalam H2O adalah 1,1% pada ~10o, dan 3,3% pada ~ 100o. |
| Ketidakcocokan | Timbal iodida memiliki daya oksidasi atau pereduksi yang lemah. Namun reaksi redoks masih bisa terjadi. Sebagian besar senyawa dalam kelas ini sedikit larut atau tidak larut dalam air. Jika larut dalam air, maka larutannya biasanya tidak sangat asam atau sangat basa. Senyawa ini tidak reaktif air. Sensitif cahaya Kontak dengan pengoksidator atau logam aktif dapat menyebabkan reaksi keras |
Our company specializes in hazardous chemicals, flammable and explosive chemicals, toxic chemicals (legal export), ultra-pure and high-purity reagents. Welcome to contact us.
Packing and shipping