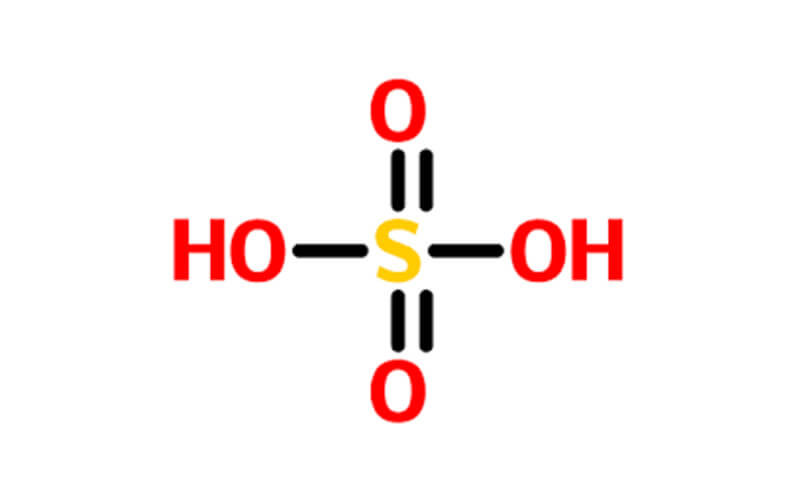
Asam sulfat7664-93-9
Penggunaan
Asam sulfat memiliki banyak kegunaan di berbagai industri, seperti produksi pupuk, produksi logam, pengolahan mineral, penyulingan minyak bumi, pengolahan air limbah, dll. Ini juga digunakan dalam produksi bahan pembersih, pewarna, pigmen, obat-obatan, deterjen, dan bahan peledak. Ini biasanya digunakan sebagai elektrolit dalam baterai timbal-asam.
- Pupuk: Sejauh ini jumlah asam sulfat terbesar digunakan untuk membuat asam fosfat, yang digunakan, pada gilirannya, untuk membuat pupuk fosfat, kalsium dihidrogenfosfat dan amonium fosfat. Ini juga digunakan untuk membuat amonium sulfat, yang merupakan pupuk yang sangat penting dalam kekurangan belerang.
- Agen pembersih industri: Asam sulfat digunakan dalam jumlah besar oleh industri pembuatan besi dan baja untuk menghilangkan oksidasi, karat, dan penskalaan dari lembaran gulung dan billet sebelum dijual ke industri mobil dan peralatan utama. Hidrogen peroksida (H2O2) dapat ditambahkan ke asam sulfat untuk menghasilkan larutan piranha, larutan pembersih yang kuat namun sangat beracun yang dapat digunakan untuk membersihkan permukaan substrat. Larutan piranha biasanya digunakan dalam industri mikroelektronika, dan juga di laboratorium untuk membersihkan barang pecah belah.
- Pengolahan logam: Ini banyak digunakan dalam pengolahan logam misalnya dalam pembuatan tembaga dan pembuatan seng dan dalam membersihkan permukaan lembaran baja, yang dikenal sebagai ‘pengawetan’, sebelum ditutup dengan lapisan timah tipis, yang digunakan untuk membuat kaleng untuk makanan.
- Katalisator: Asam sulfat dapat digunakan sebagai katalis asam dalam banyak reaksi organik. Ini mencakup nitrasi benzena, hidrasi etena untuk memproduksi etanol, dan reaksi baik untuk menghasilkan ester maupun menghidrolisisnya dalam kondisi asam.
- Elektrolit: Asam sulfat bertindak sebagai elektrolit dalam baterai timbal-asam (akumulator timbal-asam): Pada anoda: Pb + SO42− ? PbSO4 + 2 e− Pada katoda: PbO2 + 4 H+ + SO42− + 2 e− ? PbSO4 + 2 H2O; Keseluruhan: Pb + PbO2 + 4 H + + 2 SO42 − ? 2 PbSO4 + 2 H2O
- Penggunaan domestik: Asam sulfat pada konsentrasi tinggi sering kali menjadi bahan utama dalam pembersih saluran pembuangan asam[9] yang digunakan untuk menghilangkan minyak, rambut, kertas tisu, dll. Mirip dengan versi alkalinya, pembuka saluran pembuangan semacam itu dapat melarutkan lemak dan protein melalui hidrolisis. Selain itu, karena asam sulfat pekat memiliki sifat dehidrasi yang kuat, asam sulfat juga dapat menghilangkan kertas tisu melalui proses dehidrasi. Karena asam dapat bereaksi dengan air dengan kuat, pembuka pembuangan asam tersebut harus ditambahkan perlahan ke dalam pipa yang akan dibersihkan.
- Lain: Fluorapatit diolah dengan 93% asam sulfat untuk menghasilkan kalsium sulfat, hidrogen fluorida (HF) dan asam fosfat. HF dihilangkan sebagai asam fluorida. Keseluruhan proses dapat direpresentasikan sebagai: Ca5F(PO4)3 + 5 H2SO4 + 10 H2O → 5 CaSO4•2 H2O + HF + 3 H3PO4; Kegunaan penting lainnya untuk asam sulfat adalah untuk pembuatan aluminium sulfat, juga dikenal sebagai alumni pembuat kertas. 2 AlO(OH) + 3 H2SO4 → Al2(SO4)3 + 4 H2O; Asam sulfat juga penting dalam pembuatan larutan zat warna, pigmen dan obat-obatan. Terlebih lagi, asam sulfat dapat digunakan dalam pengolahan mineral, penyulingan minyak bumi dan pengolahan air limbah.
Bahaya kesehatan
Korosif pada semua jaringan tubuh. Menghirup uap dapat menyebabkan kerusakan paru-paru yang serius. Kontak dengan mata dapat mengakibatkan hilangnya penglihatan total. Kontak kulit dapat menghasilkan nekrosis parah. Jumlah fatal untuk orang dewasa: antara 1 sendok teh dan setengah ons bahan kimia pekat. Bahkan beberapa tetes bisa berakibat fatal jika asam mendapatkan akses ke trakea. Paparan kronis dapat menyebabkan trakeobronkitis, stomatitis, konjungtivitis, dan gastritis. Perforasi lambung dan peritonitis dapat terjadi dan dapat diikuti oleh kolaps peredaran darah. Syok peredaran darah seringkali menjadi penyebab langsung kematian. Mereka yang menderita penyakit pernapasan, pencernaan, atau saraf kronis dan penyakit mata dan kulit berisiko lebih besar.
Asam sulfat pekat adalah cairan yang sangat korosif yang dapat menyebabkan luka bakar parah dan dalam saat kontak kulit. Asam pekat menghancurkan jaringan karena aksi dehidrasinya, sedangkan H 2SO4 encer bertindak sebagai iritasi kulit karena karakter asamnya. Kontak mata dengan H2SO4 pekat menyebabkan luka bakar parah, yang dapat mengakibatkan kehilangan penglihatan permanen; kontak dengan H2SO4 encer menghasilkan efek yang lebih transien dari mana pemulihan dapat selesai. Kabut asam sulfat sangat mengiritasi mata, saluran pernapasan, dan kulit. Karena tekanan uapnya yang rendah, bahaya inhalasi utama dari asam sulfat melibatkan menghirup kabut asam, yang dapat mengakibatkan iritasi pada saluran pernapasan bagian atas dan erosi permukaan gigi. Paparan inhalasi yang lebih tinggi dapat menyebabkan iritasi paru-paru sementara dengan kesulitan bernapas. Menelan asam sulfat dapat menyebabkan luka bakar parah pada selaput lendir mulut dan kerongkongan. Pengujian pada hewan dengan asam sulfat tidak menunjukkan efek karsinogenik, mutagen, embriotoksik, atau reproduksi. Paparan kronis kabut asam sulfat dapat menyebabkan bronkitis, lesi kulit, konjungtivitis, dan erosi gigi.
Asam sulfat pekat adalah cairan yang sangat korosif yang dapat menyebabkan luka bakar parah dan dalam pada jaringan. Itu dapat menembus kulit dan menyebabkan nekrosis jaringan. Efeknya mungkin mirip dengan luka bakar termal. Kontak dengan mata dapat menyebabkan hilangnya penglihatan permanen.
Menghirup uap atau kabutnya dapat menghasilkan penyempitan bronkial yang parah. Karena tekanan uap asam sulfat dapat diabaikan, <0,001 torr pada 20 ° C (68 ° F), bahaya inhalasi rendah. Namun, kabut asam, memiliki ukuran partikel <7 μm, dapat menembus saluran pernapasan bagian atas dan saluran hidung. Paparan asam manusia pada konsentrasi 5 mg / m3di udara yang dihasilkanbatuk. Pada konsentrasi <1 mg/m3, tidak ada iritasi. Paparan kronis terhadap kabut asam sulfat dapat menghasilkan bronkitis, konjungtivitis, lesi kulit, dan erosi gigi. Sering kontak dengan asam encer dapat menyebabkan dermatitis kulit.
Nilai LD50, oral (tikus): 2140 mg / kg
nilai LC50, inhalasi (tikus): 510 mg / m3/2 jam.
Perusahaan kami mengkhususkan diri dalam bahan kimia berbahaya, bahan kimia yang mudah terbakar dan meledak, bahan kimia beracun (ekspor legal), reagen ultra-murni dan kemurnian tinggi. Selamat datang untuk menghubungi kami.
Pengepakan dan pengiriman