Структурный состав HF: формула фтористоводородной кислоты и ее молекулярная масса
Фтористоводородная кислота (HF) выделяется как химическое соединение, широко используемое в различных отраслях промышленности, и обладает уникальным набором свойств. Базовое понимание его формулы, структуры и состава имеет первостепенное значение для понимания его поведения и обеспечения безопасного обращения с ним. В этом всеобъемлющем руководстве мы подробно разберем формулу фтористоводородной кислоты, углубимся в ее структурное устройство, выясним ее элементный состав и точно рассчитаем ее молекулярную массу.

Расшифровка формулы фтористоводородной кислоты: HF
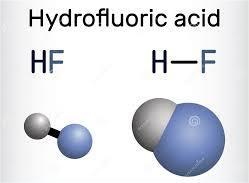
Химическая формула фтористоводородной кислоты удивительно проста: HF. Эта краткая запись показывает, что каждая отдельная молекула фтористоводородной кислоты состоит из одного атома водорода (H) и одного атома фтора (F), непосредственно связанных друг с другом.
- Водород (H): Будучи первым элементом периодической таблицы, водород является неметаллом, относящимся к группе 1. Его атомный номер равен 1, что означает один протон и один электрон в нейтральном состоянии.
- Фтор (F): Высокореакционноспособный неметалл, относящийся к группе 17, также известный как галогены. Фтор может похвастаться атомным номером 9, указывающим на девять протонов и девять электронов. Обладая семью валентными электронами в самой внешней оболочке, фтор проявляет высокую степень электроотрицательности, стремясь получить еще один электрон для достижения стабильного октета.
Формула HF кратко описывает эту двухатомную молекулу, где одинокий атом водорода образует одну ковалентную связь с одним атомом фтора.
Понимание структуры и связывания HF
Структура отдельной молекулы фтористоводородной кислоты линейна, при этом атомы водорода и фтора выровнены по прямой линии, непосредственно соединены своей химической связью. Связь между водородом и фтором представляет собой ковалентную связь, возникающую в результате совместного использования пары электронов между двумя атомами.
Тем не менее, история не заканчивается простой ковалентной связью. Из-за существенной разницы в электроотрицательности между водородом и фтором (фтор значительно более электроотрицателен), общая электронная пара в ковалентной связи распределяется неравномерно. Это неравное распределение приводит к образованию полярной ковалентной связи. В этой полярной связи более электроотрицательный атом фтора сильнее притягивает общие электроны, приобретая частичный отрицательный заряд (δ-), в то время как атом водорода, потеряв некоторую электронную плотность, несет частичный положительный заряд (δ+).
Эта присущая молекуле HF полярность приводит к образованию прочных межмолекулярных водородных связей как в жидкой, так и в твердой фтористоводородной кислоте. Эти водородные связи образуются между частично положительным атомом водорода одной молекулы HF и частично отрицательным атомом фтора соседней молекулы HF. В жидкой фазе эти межмолекулярные притяжения заставляют молекулы HF ассоциироваться, образуя цепи и даже циклические структуры, при этом средняя длина цепи обычно состоит из пяти-шести молекул.
Интересно, что в газообразном состоянии фтористоводородная кислота в основном существует в виде отдельных двухатомных молекул (HF). Тем не менее, даже в газовой фазе некоторые димеры (две молекулы HF, связанные вместе) и высшие полимеры могут быть обнаружены благодаря стойкому влиянию водородных связей.
Элементный состав фтористоводородной кислоты
Элементный состав фтористоводородной кислоты прост и напрямую вытекает из ее химической формулы:
- Водород (H): Составляет один атом на молекулу HF.
- Фтор (F): Составляет один атом на молекулу HF.
Чтобы понять пропорции по массе, мы рассмотрим соответствующие атомные веса.
Расчет молекулярной массы плавиковой кислоты
Молекулярная масса, также часто называемая молярной массой, фтористоводородной кислоты определяется путем суммирования атомных масс отдельных атомов, составляющих молекулу:
- Атомная масса водорода (H): примерно 1,01 атомных единиц массы (amu) или граммов на моль (г/моль)
- Атомная масса фтора (F): примерно 19,00 а.е. или грамм на моль (г/моль)
Поэтому молекулярная масса HF рассчитывается следующим образом:
Молекулярная масса (HF) = Атомная масса H + Атомная масса F Молекулярная масса (HF) = 1,01 а.е. + 19,00 а.е. Молекулярная масса (HF) ≈ 20,01 а.е.
При рассмотрении макроскопических величин молярная масса фтористоводородной кислоты составляет примерно 20,01 г/моль. Это означает, что один моль, который содержит количество молекул Авогадро (примерно 6,022 x 10²³ молекул) HF, имеет массу около 20,01 грамма.ИмяОтправить по электронной почте*Сообщение*Отправить
Основные выводы: структура и состав ВЧ
- Основной формулой фтористоводородной кислоты является HF, что указывает на прямую связь между одним атомом водорода и одним атомом фтора.
- Связь между водородом и фтором представляет собой полярную ковалентную связь из-за значительной разницы в электроотрицательности между двумя элементами.
- Фтористоводородная кислота обладает сильными межмолекулярными водородными связями, что приводит к ассоциации молекул в ее конденсированных фазах (жидкой и твердой).
- Элементный состав HF представляет собой простое соотношение атомов водорода и фтора 1:1.
- Молекулярная масса (или молярная масса) HF составляет примерно 20,01 г/моль.
Глубокое понимание структуры и состава фтористоводородной кислоты, а также ее молекулярной массы – это не просто академическое упражнение. Это критически важно для понимания его химического поведения, прогнозирования его реакционной способности и создания соответствующих протоколов безопасности при обращении с этим особенно коррозионным и реактивным веществом в его различных областях применения в химии и промышленности.
Вопросы и ответы
Какова химическая формула фтористоводородной кислоты?
Формула фтористоводородной кислоты — HF. Он имеет один атом водорода и один атом фтора.
Каковы уникальные свойства фтористоводородной кислоты?
Фтористоводородная кислота является слабой кислотой. Он обладает особым связующим свойством. Он очень коррозионный и может растворять стекло и некоторые металлы. Он также очень опасен, потому что может проникнуть через кожу. Это может привести к серьезным ожогам.
Каковы распространенные промышленные применения фтористоводородной кислоты?
Фтористоводородная кислота используется по-разному. Он используется для изготовления флюороуглеродов и травления стекла. Он также используется в производстве полупроводников и переработке минералов. Он также используется в производстве других химических веществ и лекарств.
Как сила фтористоводородной кислоты соотносится с другими кислотами?
Фтористоводородная кислота является слабой кислотой. Он не полностью разлагается в воде. Но он очень коррозионный. Даже при низких уровнях это может быть очень опасно. Он может проникнуть через кожу и повредить кости.
Каковы меры предосторожности при работе с фтористоводородной кислотой?
Работа с фтористоводородной кислотой очень опасна. Нужно надеть специальные защитные средства. Вам также нужна хорошая вентиляция и обучение. Воздействие СН может быть очень серьезным. Это может быть даже опасно для жизни. Так что нужно быть очень осторожным. Мы поддерживаем кастомизацию продукта Конкретные спецификации, марки, реагенты, сравнение цен приветствуетсяСвяжитесь с нами:https://www.yuhanchemi.com/contact
Yuhan Chemical provides various sulfuric acids in various concentration levels. If you have any needs, please contact:https://www.yuhanchemi.com/ultra-pure-sulfuric-acid
Yuhan Chemical, focusing on chemical raw materials:https://www.yuhanchemi.com/about-us