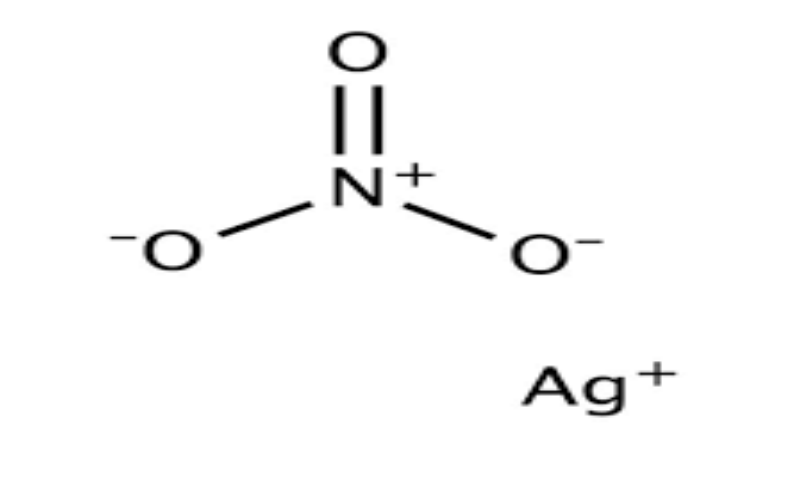
Bạc Nitrat (AgNO₃)7761-88-8
Tính chất vật lý
- Xuất hiện: Tinh thể không màu, trong suốt, hình thoi hoặc bột tinh thể màu trắng.
- Mật độ: 4,35 g / cm³ ở 20 °C.
- Điểm nóng chảy: 212 °C.
- Điểm sôi: Phân hủy ở 444°C để tạo thành bạc kim loại, nitơ điôxit và oxy.
- Độ hòa tan:
- Hòa tan cao trong nước và amoniac.
- Hòa tan nhẹ trong etanol, không hòa tan trong axeton, benzen và axit sunfuric đậm đặc.
- pH: Dung dịch nước có tính axit yếu (pH = 5-6).
Tính chất hóa học
- Chất oxy hóa: Chất oxy hóa mạnh có thể đẩy nhanh quá trình đốt cháy và gây cháy nổ khi trộn với vật liệu hữu cơ hoặc chất khử.
- Độ nhạy sáng: Các tinh thể nitrat bạc nguyên chất ổn định trong ánh sáng, nhưng nó bị phân hủy khi có chất hữu cơ, chuyển sang màu xám hoặc đen.
- Phản ứng:
- Hình thành kết tủa với halogenua (ví dụ: AgCl), sunfua (ví dụ: Ag₂S) và cromat (ví dụ: Ag₂CrO₄).
- Tạo thành các ion phức hợp với amoniac (ví dụ: Ag (NH₃) ₂⁺), xyanua (ví dụ: [Ag (CN) ₂] ⁻) và thiosulfat (ví dụ: [Ag (S₂O₃) ₂] ³⁻).
- Phản ứng với các chất khử (ví dụ: hydrazine, axit phốt pho) để tạo thành bạc kim loại.
Sử dụng
- Nhiếp ảnh: Được sử dụng làm nguyên liệu cho vật liệu cảm quang halogen bạc.
- Điện tử: Được sử dụng trong sản xuất chất kết dính dẫn điện và bạc các linh kiện điện tử.
- Thuốc: Được sử dụng như một chất khử trùng và đốt cháy để điều trị mụn cóc, loét và quá mẫn cảm với răng.
- Các ứng dụng khác:
- Được sử dụng trong sản xuất gương, mạ bạc và như một thuốc thử phân tích.
- Được sử dụng trong sản xuất muối bạc và chất xúc tác khác.
An toàn và Nguy hiểm
- Rủi ro sức khỏe: Ăn mòn mạnh da và niêm mạc; gây kích ứng, loét và đổi màu.
- Nguy cơ cháy nổ: Không cháy nhưng đẩy nhanh quá trình đốt cháy các vật liệu dễ cháy. Hỗn hợp với các chất khử (ví dụ: phốt pho, thiếc (II) clorua) có thể phát nổ.
- Bảo quản và xử lý: Bảo quản nơi khô ráo, thoáng mát, tránh xa các vật liệu nhẹ và hữu cơ. Sử dụng thiết bị bảo hộ khi xử lý.
Cân nhắc về môi trường
- Độc tính: Phân hủy tạo ra khói oxit nitơ độc hại (NOₓ).
- Xử lý: Vứt bỏ theo quy định của địa phương để tránh ô nhiễm môi trường.
Chuẩn bị
Bạc nitrat thường được điều chế bằng cách hòa tan bạc kim loại trong axit nitric loãng, sau đó bay hơi và kết tinh lại.
- Phản ứng: Ag + 2HNO₃ → AgNO₃ + H₂O + NO₂↑.
Công ty chúng tôi chuyên về hóa chất nguy hiểm, hóa chất dễ cháy nổ, hóa chất độc hại (xuất khẩu hợp pháp), thuốc thử siêu tinh khiết và có độ tinh khiết cao. Chào mừng bạn đến liên hệ với chúng tôi.
Đóng gói và vận chuyển