ลิเธียมซัลไฟด์12136-58-2
แอตทริบิวต์ของผลิตภัณฑ์
| จุดหลอมเหลว | >900 องศาเซลเซียส |
| ความหนาแน่น | 1.66 ก./มล. ที่ 25 °C (สว่าง) |
| อุณหภูมิในการจัดเก็บ | 2-8 องศาเซลเซียส |
| ฟอร์ม | แป้ง |
| ความถ่วงจําเพาะ | 1.66 |
| สี | เหลือง |
| ความสามารถในการละลายน้ํา | ละลายในน้ําและเอทานอล |
| โครงสร้างผลึก | ประเภท CaF2 ย้อนกลับ |
| ใจน้อย | ไวต่อความชื้น |
| ระบบคริสตัล | ลูกบาศก์ |
| กลุ่มอวกาศ | เอฟเอ็ม 3 ม |
| ค่าคงที่ตาข่าย | a/nmb/nmc/nmα/oβ/oγ/oV/nm30.57180.57180.57189090900.187 |
| อินชไอ | InChI=1S/2Li.S |
| อินชิคิกี้ | ZWDBUTFCWLVLCQ-UHFFFAOYSA-N |
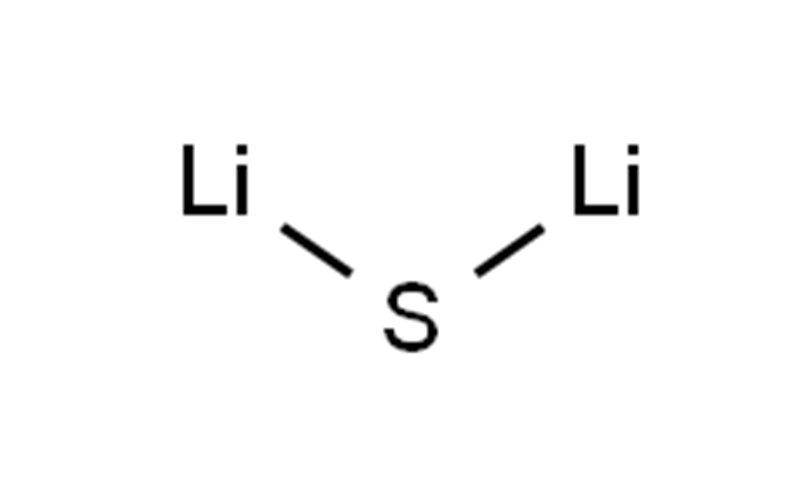
| รอย ยิ้ม | S([Li])[Li] |
ข้อมูลด้านความปลอดภัย
| ริดาดร์ | สหประชาชาติ 2923 8/PG 2 |
| WGK เยอรมนี | 3 |
| อาร์ทีเอส | OJ6439500 |
| ทีเอสซีเอ | ใช่ |
| ระดับอันตราย | 8 |
| กลุ่มบรรจุภัณฑ์ | ครั้งที่สอง |
การใช้และการสังเคราะห์ลิเธียมซัลไฟด์
| คุณสมบัติทางเคมี | ลิเธียมซัลไฟด์เป็นสารประกอบอนินทรีย์ที่มีสูตร Li2S มันตกผลึกในลวดลายแอนตี้ฟลูออไรต์ ซึ่งอธิบายว่าเป็นเกลือ (Li+)2S2−มันก่อตัวเป็นผงละลายสีเหลือง-ขาวที่เป็นของแข็งในอากาศ มันไฮโดรไลซ์เพื่อปล่อยไฮโดรเจนซัลไฟด์ (กลิ่นไข่เน่า) ลิเธียมซัลไฟด์เตรียมโดยการบําบัดลิเธียมด้วยกํามะถันปฏิกิริยานี้ดําเนินการได้อย่างสะดวกในแอมโมเนียปราศจากน้ําสารเติมดักต์ไตรเอทิลโบเรนที่ละลายน้ํา THF ของลิเธียมซัลไฟด์สามารถสร้างได้โดยใช้ซุปเปอร์ไฮไดรด์ ลิเธียมซัลไฟด์ (Li2S) ถือเป็นวัสดุแคโทดที่มีแนวโน้มสําหรับความจุทางทฤษฎีสูง |
| คุณสมบัติทางกายภาพ | ลิเธียมซัลไฟด์ Li2S เป็นเซมิคอนดักเตอร์ต่อต้านฟลูออไรต์ที่มีช่องว่างวงดนตรี 3.865 eV นอกจากนี้ยังมีจํานวนเวเลนซ์อิเล็กตรอน Ne และเลขอะตอม Z เท่ากันทุกประการกับแมกนีเซียมไดโบไรด์ MgB2 ทั้งสองมีน้ําหนักสูตรเกือบเท่ากันสิ่งนี้ทําให้ Li2S มีคุณสมบัติเป็นวัสดุคล้ายแมกนีเซียมไดโบไรด์ Li2S ผ่านการทดสอบเฉพาะวัสดุคํานวณแบบเดียวกับ MgB2 ลิ เธียมซัลไฟด์เป็นวัสดุที่ได้รับการศึกษาอย่างมาก Li2S สามารถมีได้สองรูปแบบ: ออร์โธทอมบิกและลูกบาศก์รูปแบบออร์โธไรมบิกอยู่ในกลุ่มอวกาศ Pmnb และมีขนาด: a = 3.808Å;b = 6.311Å;ค = 7.262Å มีความหนาแน่น 1.75g/cm3 รุ่นลูกบาศก์มีความหนาแน่น 1.63g/ cm3 อยู่ในกลุ่มอวกาศ Fm-3m และมีขนาดลูกบาศก์ 4.046Å โครงสร้างอิเล็กทรอนิกส์และความหนาแน่นของสถานะบ่งชี้ว่าลูกบาศก์ Li2S เป็นเซมิคอนดักเตอร์ช่องว่างแถบทางอ้อมที่มีช่องว่างแถบความถี่ 3.865 eV ลิเธียมซัลไฟด์ละลายระหว่าง 900 – 975 องศาเซนติเกรด |
| ใช้ | ลิเธียมซัลไฟด์ได้รับการศึกษาว่าเป็นตัวนํายิ่งยวดที่คล้าย MgB2 นอกจากนี้ยังใช้เป็นวัสดุแคโทดในแบตเตอรี่ลิเธียมกํามะถันแบบชาร์จไฟได้ |
| ใช้ | ลิเธียมซัลไฟด์ (Li2S) เป็นผลิตภัณฑ์ที่ออกแบบมาเป็นพิเศษสําหรับใช้ในแบตเตอรี่ประสิทธิภาพสูง ซึ่งสามารถนําไปใช้เป็นวัสดุอิเล็กโทรดหรือเป็นสารตั้งต้นสําหรับอิเล็กโทรไลต์ที่เป็นของแข็งในฐานะที่เป็นวัสดุอิเล็กโทรดไม่เพียงแต่มีความจุสูง แต่ยังเอาชนะปัญหามากมายที่เกิดจากอิเล็กโทรดกํามะถันบริสุทธิ์อีกด้วย ลิเธียมซัลไฟด์เป็นเซมิคอนดักเตอร์ป้องกันฟลูออไรต์ (แบนด์แกป 3.865eV)มีอยู่ในโครงสร้างออร์โธโรมบิกและลูกบาศก์ความหนาแน่นของโครงสร้างออร์โธโรมบิกและลูกบาศก์คือ 1.75g/cm3 และ 1.63g/cm3 ตามลําดับ ลิเธียมซัลไฟด์ได้รับการศึกษาว่าเป็นตัวนํายิ่งยวดคล้าย MgB2 นอกจากนี้ยังใช้เป็นวัสดุแคโทดในแบตเตอรี่ลิเธียมซัลเฟอร์แบบชาร์จไฟได้ |
| การตระเตรียม | ลิเธียมซัลไฟด์ Li2S เกิดขึ้นในปฏิกิริยาของลิเธียมกับกํามะถันในแอมโมเนียเหลวโดยการสลายตัวของเอทานอลของลิเธียมไฮโดรเจนซัลไฟด์กับลิเธียมเอทานอลและเมื่อเร็ว ๆ นี้โดยปฏิกิริยาของไฮโดรเจนซัลไฟด์กับลิเธียมอะไมเลตเพื่อให้ได้ลิเธียมไฮโดรเจนซัลไฟด์ LiSH ซึ่งถูกย่อยสลายด้วยความร้อนในสุญญากาศเพื่อให้ได้ซัลไฟด์ลิเธียมซัลไฟด์ปราศจากน้ําคุณภาพสูงมากอาจเตรียมโดยปฏิกิริยาของโลหะลิเธียมและไฮโดรเจนซัลไฟด์ในเตตระไฮโดรฟรานหากใช้ความระมัดระวังในการแยกน้ําผลิตภัณฑ์ปฏิกิริยาจะถูกกรองจากตัวกลางปฏิกิริยาและแห้งด้วยสุญญากาศเพื่อขจัดเตตระไฮโดรฟลูฟาแรนและย่อยสลายลิเธียมไฮโดรเจนซัลไฟด์จํานวนเล็กน้อยซึ่งก่อตัวขึ้นมีรายงานว่าลิเธียมซัลไฟด์มีโครงสร้างต่อต้านฟลูออไรต์ลิเธียมซัลไฟด์ถูกไฮโดรไลซ์ได้ง่ายแม้โดยน้ําในอากาศทําให้เกิดไฮโดรเจนซัลไฟด์ซัลไฟด์ยังทําปฏิกิริยากับกํามะถันเพื่อสร้างโพลีซัลไฟด์หลายชนิด |
| คําอธิบายทั่วไป | ลิเธียมซัลไฟด์เป็นเซมิคอนดักเตอร์ต่อต้านฟลูออไรต์ (แบนด์แกป 3.865eV)มีอยู่ในโครงสร้างออร์โธไรมบิกและลูกบาศก์ความหนาแน่นของโครงสร้างออร์โธโรมบิกและลูกบาศก์คือ 1.75g/cm3 และ 1.63g/cm3 ตามลําดับ |
| พิษวิทยา | ลิเธียมไอออนในปริมาณมากทําให้เกิดอาการวิงเวียนศีรษะและกราบ และอาจทําให้ไตเสียหายได้หากการบริโภคโซเดียมมีจํากัดมีรายงานการขาดน้ํา น้ําหนักลด ผลกระทบทางผิวหนัง และต่อมไทรอยด์ผิดปกติผลกระทบของระบบประสาทส่วนกลาง ซึ่งรวมถึงการพูดไม่ชัด ตาพร่ามัว การสูญเสียประสาทสัมผัส ataxia และอาการชักอาจเกิดขึ้นได้อาการท้องร่วง อาเจียน และผลกระทบของระบบประสาทและกล้ามเนื้อ เช่น ตัวสั่น โคลนัส และปฏิกิริยาตอบสนองที่กระตือรือร้นอาจเกิดขึ้นจากการสัมผัสกับลิเธียมไอออนซ้ําๆ |
| วิธีการผลิต | รวมองค์ประกอบโดยตรง นั่นคือ ผสมลิเธียมปริมาณสัมพันธ์และกํามะถัน ให้ความร้อนในเบ้าหลอมนิกเกิลภายใต้บรรยากาศเฉื่อย (อาร์กอนหรือฮีเลียม) จนกว่าจะละลาย และรอจนกว่าจะเกิดการหลอมละลายที่สม่ําเสมอลิเธียมซัลเฟตยังสามารถลดลงได้ด้วยผงคาร์บอนใช้ส่วนผสมของลิเธียมซัลเฟต 100 กรัมและผงคาร์บอน 436 กรัม แล้วอุ่นในเตาไฟฟ้าจนกว่าจะเกิดการหลอมละลายสม่ําเสมอผลิตภัณฑ์นี้ละลายได้ดีในน้ํา และลิเธียมไฮดรอกไซด์และลิเธียมไฮโดรซัลไฟด์เกิดขึ้นในสารละลายที่เป็นน้ํา ซึ่งมีความเป็นด่างสูง: Li2S+H2OLiOH+LiHS กรดไฮโดรคลอริกและลิเธียมซัลไฟด์ทําปฏิกิริยาอย่างรวดเร็วเมื่อเย็นเพื่อผลิตไฮโดรเจนซัลไฟด์และลิเธียมคลอไรด์: Li2S+HClLiCl+2H2S |